Вправа при вивченні теми "Ферум. Залізо. Властивості, добування. Застосування" для використання на уроці хімії є вправою-учасницею Всеукраїнського конкурсу на кращу вправу з інтеграції медіаграмотності для учнів 7-8 класів.
Авторка: Калинич Людмила Андріївна, учителька хімії та біології Криворізьскої гімназії №127 Криворізької міської ради Дніпропетровської області.
Запропанований інтегрований урок – це міждисциплінарне об’єднання уроків з хімії, біології, історії, географії, фізики, літератури, медицини, екології, спрямоване на комплексне пізнання запропанованої теми, законів, ідей з метою отримання школярами більш поглибленого розуміння і закріплення знань про Ферум-хімічний елемент і просту речовину Залізо. А також можливість STEAM-діяльності, а саме удосконалення знань для людей, що мають особливе ХОБІ - вирощування кристалів, а також тих, хто любить створювати моделі молеку, атомів. Урок має і профорієнтаційний матеріал, важливий для нашого регіону
Урок розрахований на 2 години.
Міжпредметна інтеграція, зокрема -
Історія – виникнення і розвиток гірничодобувної промисловості регіону
Географія – різноманітність і цінність корисних копалинх,
Біологія – значення заліза для живих організмів.
Фізика- будова атома Феруму, фізичні властивості заліза.
Хімія- хімічні властивості, застосування, значення заліза.
Література- легенди про Рудану, вірші про залізо.
Медицина, екологія- про нестачу заліза в живих організмах, способи усунення, вплив на природу і здоров'я результатів добування руди і переробки металів .
Хобі – правила і умови вирощування кристалів з солей Феруму.
STEM- моделювання атомів Феруму, молекул, кристалічних граток. Цей урок можна використовувати
- на уроках хімії - при вивченні тем «Металічні елементи», «Метали побічних підгруп», «Ферум. Залізо».
- цікавим і корисним буде поданий матеріал для профорієнтаційної роботи при ознайомленні з професіями, пов’язаними з добуванням і переробкою корисних копалин, в металургійній і горнодобувній галузях,
- для бажаючих експериментаторів, в області хімії, вирощувати гарні, різнокольорові кристали з солей Феруму.
- моделювання граток, атомів.
При створенні уроку використані:
- сервіс- Coggle,
- технологія «Сторістелінг»
- опитники на платформах «Kahoot», «LearningApps».
- генератор QR-code
- Вікіпедія
- Ютуб- канал
Цей урок можна вважати інноваційним тому, що викладена цікава інформація на ментальній карті, містить активні посилання на сайти, ютуб канал, платформи «Kahoot», «LearningApps», Вікіпедію.
Цікаве проведення уроку буде при наявності інтерактивної дошки чи проектора з доступним інтернетом.
Дуже доречно викладений матеріал можна використовувати під час дистанційного навчання. Підібрані фільми, тексти доступно пояснюють подану тему. Цікаво представлена інформація про професії, пов’язані з темою уроку. Заоохочуючею і пізнавальною є профорієнтаційна гра «Залізна логіка», яка допоможе вивчити і закріпити знання з теми.
Тема уроку: Ферум. Залізо. Властивості, добування, застосування
(спарений урок- 2 години)
Освітньо – виховні завдання теми: створити комфортні умови для навчання, за яких кожен учень відчуває свою успішність, інтелектуальну спроможність, самостійність.
Навчальна мета: опанування цього матеріалу надасть учням можливість:
Знаннєвий компонент: знати положення Феруму в періодичній системі хімічних елементів, будову атома, поширення в земній корі, фізичні та хімічні властивості заліза, основні галузі добування і переробки, його застосування;
називати основні природні сполуки Феруму та продукти реакцій в які вступає залізо, залежність будови і властивостей на прикладі сполук Феруму(II) і Феруму (III); застосування заліза та сполук Феруму, поширення в земній корі; називати основні природні сполуки Феруму, перелік професій, повязаних з добуванням руди, металів іх переробкою
Діяльнісний компонент: складати рівняння реакцій, які характеризують хімічні властивості заліза та його сполук, експериментально визначати сполуки Феруму(II) та Феруму (III)., навчитися вирощувати кристали з солей Феруму, моделювати гратки атомів, сполук.
Ціннісний компонент: оцінювати біологічне значення Феруму, його вплив на здоров’я людини.
Виховний компонент: сформувати науковий світогляд учнів при вивченні фізичних та хімічних властивостей заліза та його сполук, їх застосування; сприяти екологічному вихованню. Виховувати в учнів національну свідомість, самосвідомість та ментальність, провідні риси громадянина своєї держави, любов до рідної країни, до української мови, до свого народу, до міста Кривого Рогу. Виховувати в учнів любов до рідної природи, повагу до оточуючого середовища.
Розвиваючий компонент: розвивати спостережливість учнів на уроці хімії; розвивати пізнавальний інтерес учнів до предмету; розвивати навички складання рівнянь хімічних реакцій на прикладі хімічних властивостей заліза та його сполук;
розвивати такі мисленнєві операції : вміння порівнювати, узагальнювати, робити висновки; розвивати такі мисленнєві операції : вміння порівнювати, узагальнювати, робити висновки, розвивати самостійність під час виконання завдань.
Тип уроку: Урок засвоєння нових знань та вмінь.
Міжпредметні зв’язки: біологія, історія, географія, фізика, література, екологія, медицина
Обладнання: підручники, таблиці- періодична система хімічних елементів, таблиця розчинності, ряд активності металів, зразки виробів із заліза, магніт, пластилін і зубочистки, нитки, мультимедійне обладнання, наявність інтернету.
Хід уроку
І Організаційний момент.
Перевірка присутності учнів на уроці та готовності їх до уроку.
Створення позитивного налаштування. Проведення вправи «Подаруй посмішку» для цього попросити учнів посміхнутися один одному, сусіду через парту, вчительці, дошці, портрету Менделєєва Д.І, тощо.
ІІ. Актуалізація опорних знань.
Бліц-опитування
3.Які ви знаєте елементи,що входять до побічних підгруп?
ІІІ. Мотивація навчальної діяльності. Повідомлення теми, мети уроку
Сьогодні познайомимося з елементом який необхідний для всіх живих організмів і без нього неможливо уявити свого життя.
Щоб назвати цей елемент, вам треба відгадати загадку:
Я поширений в природі,
Кожному стаю в пригоді.
Де мне зустріти можна,
З вас, напевне, знає кожен.
Магнетит і гематит,
Лімонит і сидерит-
Руди ці – матусі рідні,
А татусь – метеорит.
Я умію воювати,
Але вмію й будувати
Рейки, кораблі, машини,
Теплоходи і турбіни.
Кров чому у вас червона?
Бо в крові є мої йони.
І без мене Ні- врожаю,
І про це я точно знаю.
Вголос мовте для загалу
Назву чорного металу.
Так це дійсно- Залізо
На дошці висвітлюється ментальна карта.

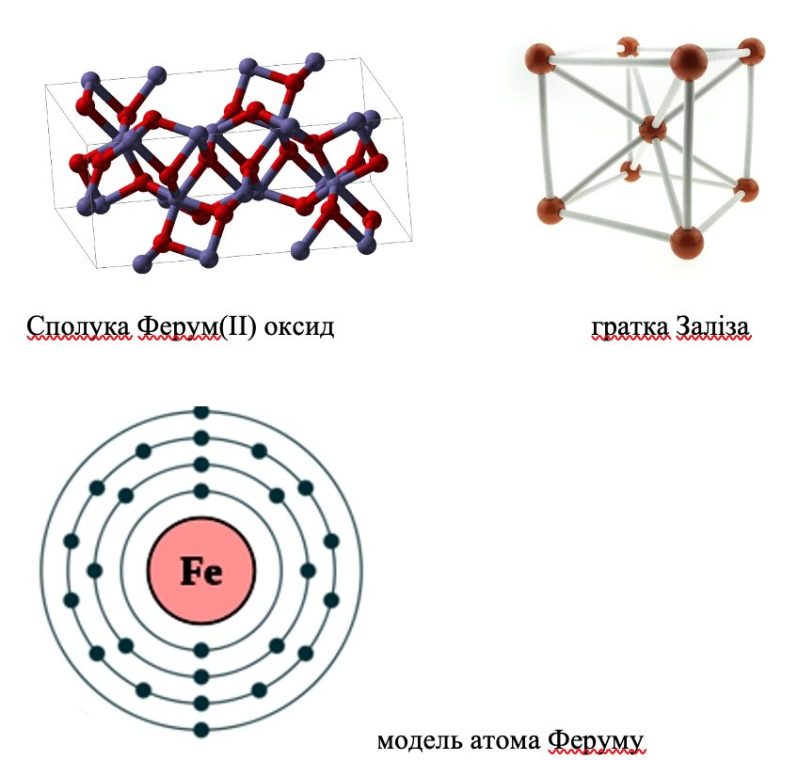
1 Положення в ПС, будова атома
Ферум - металічний елемент VІІІ групи побічної підгрупи, ІV періоду. Зовнішній енергетичний рівень атома Феруму має типову для металічних елементів будову – на ньому розміщено 2 s – електрони. Водночас на d – підрівні третього енергетичного рівня міститься 6 електронів.
У сполуках Ферум проявляє ступені окиснення +2, +3, хоча за певних умов можна добути речовини зі ступенем окиснення +6.
Перегляд відеофрагменту https://www.youtube.com/watch?v=S4pB6x3EA4o&t=15s
На підставі положення Феруму в Періодичній системі та будові атома ми можемо зробити наступний прогноз щодо хімічного елемента Ферум та простої речовини заліза:
а) Ферум – металічний елемент, що виявляє у сполуках змінні валентності та ступені окиснення
б) залізо – метал, який у хімічних реакція виявляє відновні властивості;
в) оксид і гідроксид Феруму зі ступінню окиснення +2 повинні виявляти основні властивості, а з ступінню окиснення +3 – амфотерні.
STEM-пауза Моделюємо будову атома, моделі сполук Fe2O3 та FeO, для цього використовуємо пластілін і зубочистки, нитки або інший матеріал(цукерки, зефір, кусочки яблука, тощо)
2 Поширення Феруму в природі.
Легенда про Рудану
https://www.youtube.com/watch?v=zZpv7pwrefQ)
Історична назва https://sites.google.com/site/ferum5341531/
Ферум за поширеністю в природі займає друге місце серед металічних елементів (після алюмінію). На нього припадає 5 % від маси земної кори. За вмістом в земній корі Ферум займає 4-е місце.
В природі у вільному стані Ферум не зустрічається, але у вигляді простої речовини він входить до складу деяких метеоритів. В метеоритах міститься від 25 до 90,85 % Феруму.Ферум входить до складу хімічно стійких сполук: солей (карбонатів, сульфідів) та оксидів:
До основних залізних руд відносяться:
Fe2O3 – червоний залізняк ( гематит)
Fe3O4 - магнітний залізняк (магнетит)
Fe2O3 · H2O – бурий залізняк (лимоніт)
FeS2 – залізний колчедан, пірит
FeCO3 – залізний шпат (сидерит)
На території України знаходяться 30% розвіданих на території СНД покладів залізних руд. Найбільші родовища відкриті в Криворізькому, Кременчуцькому та Білогірському залізорудних басейнах.
Самородне залізо - крайня рідкість, в чистому вигляді зустрічається у вигляді метеоритного заліза. Найбільший у світі залізний метеорит, який спостерігали при падінні, 18 жовтня 1916 поблизу с. Богуславки, Далекосхідного краю /метеорит розбився на 2 осколки/
Перегляд https://www.youtube.com/watch?v=jYty7ZOVTwA
3 Феруму в організмі людини і рослин
Значення заліза для людського здоров'я навряд чи можна переоцінити. Воно входить до складу більшості ферментів. Залізо є важливим мікроелементом, і надходження його має бути регулярним. Не можна допускати дефіциту, адже роль заліза в організмі людини дуже важлива.
На скільки залізо є необхідним для нашого організму зможна дізнатися опрацювавши інформацію з мережі інтернет. Для цього знадобляться мобільні телефони та програма Qr-кодів – посилання на сайт.

Перегляд відео https://www.youtube.com/watch?v=JalW76ZHDZ
Залізо відноситься до числа найважливіших біоелементів. У людському організмі воно допомагає гемоглобіну правильно функціонувати і забезпечувати клітини киснем. Практично таку ж роль воно виконує і в тканинах рослин, приймаючи участь у синтезі хлорофілу та процесі дихання.
https://www.youtube.com/watch?v=HNZnrvu1POk
4 Залізо-проста речовина Фізичні властивості
А зараз розглянемо фізичні властивості Феруму.
Чисте залізо — блискучий сріблясто-білий важкий метал.
-Густина його 7,86 т/м3.
-Температура плавлення 1538 °C.
-Залізо досить пластичне.
-Легко кується, штампується, витягується в дріт і прокатується в тонкі листи
-Притягується магнітом (парамагнетик).
- Вище температури 770 °C втрачає феромагнітні властивості.
Що таке феромагнітні властивості?
Як і в усіх металів, його фізичні властивості зумовлені металічною кристалічною граткою та металічним зв’язком.
У народному фольклорі людей різних національностей досить часто зустрічаються висловлювання про важливість і значення заліза у житті людини. Вам було підготувати прислів’я та приказки про залізо та його сплави.
Прислів’я:
«Скільки не бий по залізу, йому все дарма» (Азербайджанське)
«Терплячий навіть залізо розірве» (татарське)
«Людина міцніша за залізо, твердіша за камінь, ніжніша за троянду»(турецьке)
«З поганого заліза меча не викувати» (турецьке)
«Не гріте залізо не зігнеш» (українське)
«Залізо саме не стане м’яким» (корейське)
«Куй залізо, поки гаряче» (російське)
«Міцний як сталевий меч» (японське)
«Холодне залізо нема чого кувати» (сербське)
«У бою залізо дорожче, ніж золото» (татарське)
«Залізне здоров'я» (українське)
Хімічні властивості визначаються наявністю домішок. Чисте залізо – метал середньої активності. Біля м. Делі (Індія) стоїть залізна колона висотою 7 м і масою 6,5 т без жодних слідів корозії, хоча її вік – понад 2800 р. Колона виготовлена із заліза чистотою 99,72%, стійкого до корозії.
Залізо з високим ступенем чистоти малоактивне й не піддається корозії. Проте навіть невелика частка різних домішок збільшує активність заліза в усіх хімічних реакціях. Подібно до більшості металів залізо окиснюється киснем та іншими неметалами, вступає в реакції заміщення з кислотами і солями менш активних за нього металічних елементів, взаємодіє під час нагрівання з водою.

https://www.youtube.com/watch?v=zEbYoNjJMWE&t=1008s
(Можливі два варіанти подачи матеріалу або перегляд відеоурока)
або перегляд відеофрагментів по хімічним властивостям)
Залізо - відновник, відноситься до металів середньої активності.
Реакція з неметалами.
А) Взаємодія з киснем.
При високій температурі залізо легко сполучається з киснем, утворюючи окалину Fe3O4 (FeO ∙ Fe2O3). В атмосфері кисню розжарена залізна дротина горить яскравим полум'ям:
3Fe + 2O2 = Fe3O4
https://www.youtube.com/watch?v=8CfN3NQfWK0 (відео горіння заліза в кисні)
Б) Взаємодія з хлором.
При нагріванні залізо може легко реагувати з хлором, сіркою та іншими неметалами:
https://www.youtube.com/watch?v=x0792Y7njow (відео взаємодії заліза з хлором російською мовою)
Запишіть рівняння реакції взаємодії заліза з хлором.
Зверніть увагу, що в цій реакції, оскільки Хлор сильний окисник, ступінь окиснення Феруму +3.
В) Взаємодія з сіркою.
https://www.youtube.com/watch?v=nxX-4HDEpmY (відео взаємодії заліза з сіркою).
Запишіть рівняння реакції взаємодії заліза з сіркою.
В цій реакції, оскільки Сульфур менш сильний окисник, ступінь окиснення Феруму +2.
Реакції зі складними речовинами.
А) Взаємодія з водою.
Ця реакція відбувається при нагріванні (залізо-паровий спосіб):
3Fe + 4H2O = Fe3O4+ 4H2
Б) Взаємодія з кислотами.
В електрохімічному ряді напруг залізо стоїть лівіше від водню, тому воно легко реагує з розведеними кислотами виявляючи при цьому ступінь окиснення +2 (з розбавленою нітратною кислотою, як сильним окисником, Ферум виявляє ступінь окиснення +3, а з дуже розбавленою +2).
Запишіть рівняння реакції взаємодії заліза з розчинами хлоридної та сульфатної кислот.
З розведеною нітратною кислотою залізо теж легко реагує:
Fe + 4HNO3 = Fe (NO3)3 + 2H2O + NO ↑
Треба мати на увазі, що продукт відновлення Нітрогену залежно від розведення кислоти може змінюватися з відповідним зменшенням ступеня окиснення.
Реакція Fe з концентрованими кислотами HNO3, H2SO4 на холоді не відбувається (вони пасивують залізо). Завдяки цьому концентровану нітратну і концентровану сульфатну кислоту можна зберігати і транспортувати в залізній тарі
Але при нагріванні:
2Fe + 6H2SO4 = Fe2(SO4)3 + 3SO2 + 6H2O;
Fe + 6HNO3 = Fe (NO3)3 + 6H2O + 3NO2 ↑
Продуктами цих реакцій є не водень, а нітроген(ІІ)оксид, сульфур(IV) оксид та нітроген(IV) оксиди відповідно, бо на відміну від реакцій з розбавленими хлоридною чи сульфатноюкислотами окисником виступають не катіон Гідрогену, а атоми Нітрогену чи Сульфуру звідповідними дуже високими ступенями окиснення : +5 і +6..
https://www.youtube.com/watch?v=DoIdaMmmhlQ
(відео взаємодії заліза з концентрованими кислотами)
В) Взаємодія з з розчинами солей менш активних металів.
https://www.youtube.com/watch?v=slgSCRNyvXI
(відео заміщення міді залізом)
Запишіть рівняння реакції взаємодії заліза з розчином купрум(ІІ) сульфату.
Зверніть увагу, що в цих реакціях Ферум виявляє отупінь окиснення +2.
Сполуки Феруму з валентністю ІІ.
Ферум(ІІ) оксид виявляє властивості основного оксиду, а ферум(ІІ) гідроксид – основи.
FeO + 2HCl = FeCl2 + H2O
Fe(OH)2 + H2SO4 = FeSO4 + H2O
Сполуки Феруму з валентністю ІІІ.
Ферум(ІІІ) оксид та ферум(ІІІ) гідроксид виявляють слабо амфотерні властивості. Виявляє слабкі кислотні властивості лише при сплавлянні з лугами, утворюючи солі ферити — натрій ферит NaFeO2:
Fe2O3 + 6НС1 = 2FeCl3 + 3H2O
Fe2O3 + 2NaOH (крист.) = 2NaFeO2 + Н2O
Письменник і вчений пізньої античності Пліній так висловився про роль заліза: «Рудокопи заліза видобувають для людини найкраще й найзлісніше знаряддя. Цим знаряддям прорізаємо ми землю, висаджуючи кущі, оброблюємо плодоносні сади й, обрізуючи дикі виноградні лози, примушуємо їх щоразу омолоджуватися. Цим знаряддям зводимо ми будівлі, руйнуємо камінь і використовуємо залізо на всі подібні потреби. Але тим же самим залізом вчиняємо війни, битви, грабунки й користуємося як зброєю не тільки обличчям до обличчя з ворогом, але й як летючим снарядом, що я вважаю злочинною підступністю людської винахідливості, бо для того, щоб смерть настигла людину, ми зробили її крилатою й надали залізу крила. Хай вина за це буде приписана людині, а не природі».
https://www.youtube.com/watch?v=pzxm_s-xPKE&t=26s
7. Вирощування кристалів солей заліза
Для тих, хто має таке ХОБІ
Дуже гарні кольорові кристали можна виростити з солей Феруму (ІІ) , та Феруму (ІІІ)
https://www.youtube.com/watch?v=YuNOaoZ2pl4
https://www.youtube.com/watch?v=As1aSn5L6YU
https://www.youtube.com/watch?v=XQ3duuAEkqM
https://www.youtube.com/watch?v=00JKXPXQsIs
8. Добування, переробка. (Запропонувати здобувачам освіти заздалегіть приготувати міні-проєкти стосовно підприємст міста Кривого Рогу)
https://www.youtube.com/watch?v=JMt8LOff0nU&t=39s
Загальні запаси залізних руд становлять понад 30 млрд т. Одним із найбільших у світі є Криворізький залізорудний басейн (Кривбас). Він охоплює низку родовищ, що тягнуться смугою завдовжки понад 100 км через Дніпропетровську, Кіровоградську та Миколаївську області. Промислове освоєння басейну почалося в XIX ст. Найбільше значення для господарства мають багаті (вміст заліза — понад 46 %) і високоякісні руди — червоні залізняки (гематити), які майже не містять шкідливих домішок, їх видобувають шахтним способом. Бідні руди (залізисті кварцити), що мають менший вміст заліза (від 20 %), розробляють відкритим способом (у кар'єрах). Гірничі розробки досягають глибини понад 1 000м.
На території нашої країни залізо почали добувати ще скіфи в ІІ тис. до н.е. для виготовлення зброї. Один із перших центрів, де виготовляли залізо, існував у кінці І ст.. до н.е. в Закарпатті. У Київській області знайдено фрагменти печі для виплавлення, плуги, коси, мечі, наконечники для стріл, виготовлені з місцевої болотної руди лимоніту. Виробництво заліза на території України відоме з VII — V ст. до н. е. За часів Київської Русі набув поширення сиродутний процес добування заліза, тобто відновлення залізних руд деревним вугіллям у горнах. У XIV — XVIII ст. на Поліссі, Прикарпатті, в Галичині, на Київщині здійснювалося виробництво металу в горнах і примітивних домницях. Наприкінці XVIII ст. на Поліссі з’явилися перші доменні печі, в яких з місцевих руд (зокрема, з болотних — лимоніту) виплавляли ливарний чавун на деревному вугіллі.
Заводське виробництво чорних металів в Україні набуло розвитку в другій половині ХІХ ст. одночасно з промисловою розробкою покладів кам’яного вугілля в Донбасі та залізних руд у Криворізькому і Керченському басейнах. Перша доменна піч, що працювала на кам’яному вугіллі, була споруджена в 1800 році у Луганську. Починаючи з 80-х років ХІХ ст. великі металургійні заводи, які використовували кокс, з’явились у Донбасі та Придніпров’ї.
Отже, галузь металургії є однією з найдавніших у нашій країні.
Наше Криворіжжя має найбільші підприємства гірничодобувної і металургійної галузей. Гру́па Метінве́ст — українська міжнародна гірничо-металургійна компанія, що володіє 24 підприємствами в Україні, ЄС та США, видобуває руду та вугілля, виробляє кокс, виплавляє сталь та виробляє прокат, труби тощо. Керівництво активами групи здійснює керівна компанія Групи ТОВ «Метінвест Холдинг».
https://metinvestholding.com/ua
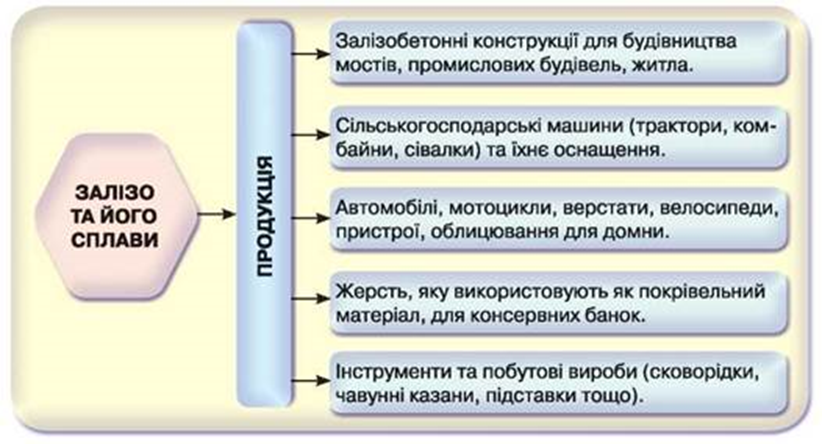
До її складу входять
ІнГЗК https://cutt.ly/tnPoyL0
ПівдГЗК https://cutt.ly/6nPogrX
ПівнГЗК https://cutt.ly/HnPi1ag
Публічне акціонерне товариство "Кривбасзалізрудком" https://cutt.ly/inPi7kM
Акціонерне товариство "СУХА БАЛКА" https://cutt.ly/FnPo57Z
9 Професії нашого регіону
У гірничодобувній промисловості !
У галузі металургії
Переглянути буклети
10 Екологічні проблеми
https://www.youtube.com/watch?v=E7bTFj06VCY
Одними із основних проблем чорної металургії є екологічні.
Що потрібно для розв'язання цієї проблеми?
ІV. Підбиття підсумків
Запропонувати здобувачам освіти виконати вправи
https://learningapps.org/view17997828
Прийом “Хрестики-нулики”.
Визначте виграшні шляхи на схемах, якщо:
а) це хімічні сполуки, що входять до складу залізних руд
| FeO | Fe(OH)3 | FeBr2 |
| FeSO4 | Fe3O4 | Fe3C |
| Fe(OH)2 | FeS | Fe2O3 |
б) це складні речовини, що належать до одного класу;
| Fe(OH)2 | FeSO4 | FeCO3 |
|
FeS |
FeCl3 | Fe2O3 |
| FeO | Fe(OH)3 | Fe3O4 |
V Рефлексія.
Прийом «Три – Два – Один». (роздаються невеликі аркуші, де є розграфлено три рядки). Пригадавши все що ви вивчили на сьогоднішньому занятті, вам потрібно виконати ще одне завдання. На аркушах, які є у вас на партах, вам потрібно записати:
- в першому рядочку Три факти, які були для вас новими, цікавими, несподіваними на занятті;
- в другому – Два факти, які здалися нецікавими, некорисними, або вже були відомі для вас;
- в третьому – Один факт, який хотілось би вивчити детальніше, поглибити свої знання.
Для закріплення матеріалу погратися в навчальну, пізнавальну, цікаву гру "Железная логика"
https://steellogic.metinvestholding.com/
Опрацювати параграфи підручника
Підготуватися до представлення проектів з тем (презентація):
Шановні освітяни, якщо ви скористаєтеся вправою для проведення заняття і заповнять коротку анкету-апробацію, отримають електронний сертифікат щодо підвищення кваліфікації.
Ще більше вправ ви зможете знайти у тулбоксі з уроками та вправами , в які інтегровані елементи медіа грамотності АУП. Ці вправи легко застосувати в уже існуючі шкільні та позакласні заняття.